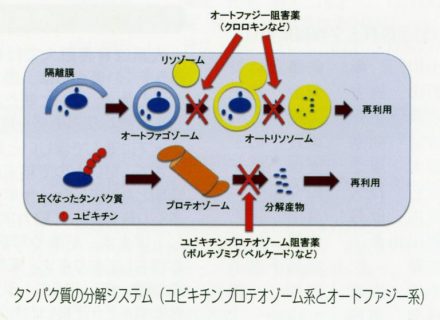
タンパク質は、生合成された後に幾つかの経路で分解されていくことが知られています。タンパク質生合成システムとタンパク質分解システムは、ある条件で平衡状態となり、常に新たなタンパク質を生合成しながら古いものを消去していくことにより生体組織の品質管理を行っていると思われます。
タンパク質分解システムは、1 ) 小さな目印タンパク質であるユビキチンを結合させたのち、プロテオゾームと呼ばれるタンパク質分解酵素群で分解していくユビキチンプロテオゾーム系、2) 隔離膜と呼ばれる二重膜で対象を覆った後にタンパク分解酵素を含むリソゾームと融合することにより分解するオートファジー系(自食作用)の2つのシステムが知られています。オートファジー系によるタンパク質分解の仕組みは、1992年に大隅先生(現東京工業大栄誉教授)のグループにより発見され、その大隅先生が2 016年のノーベル生理学·医学賞を受賞したことも記憶に新しいと思います。
タンパク質分解システムは、薬の標的としても重要です。ユビキチンプロテオゾーム系の阻害薬であるボルテゾミブ(商品名ベルケード)は、多発性骨髄腫に有効な抗がん剤として認識されています。増殖能が活発であるがん細胞は、ユビキチンプロテオゾーム系を阻害されると、異常なタンパク質の蓄積が起こり、細胞内ストレスが惹起されて細胞死が誘導されます。一方、オートファジ一阻害薬であるクロロキンは、抗マラリア剤として作用する以外に全身性エリテマトーデス(SLE) 、皮閲エリテマトーデス(CLE) などの膠原病の治療に使われています(実際に使用されている薬物はクロロキン代謝産物であるヒドロキシクロロキン)。その詳細な作用機序は、未だ不明な点が多いですが、免疫細胞の活性化ならびに炎症過程を抑制すると考えられています。そのため、タンパク質分解システムは、タンパク質の分解のみならず、様々な細胞において細胞死あるいは細胞機能を制御していると考えられ、非常にホットな領域となっています。
心臓でのタンパク質の品質管理は、主にユビキチンプロテオゾーム系を用いて行われており、この系によるタンパク質分解システムの低下は、心臓疾患と密接に関わっていることが報告されています。その一方で、オートファジー系の役割は未だに不明な点が多く、栄養が不足している状態(飢餓状態)などの過酷な状況では活性化して、タンパク質分解による栄養供給に関与すると推測されます。我々の研究室は、遺伝子改変技術を用いて、心臓だけでオートファジー系が活性化しているマウスの作製に成功しました。このマウスでは、心機能が低下し、心筋のストレスマーカーが増大していました。この結果から、オートファジーの過剰な活性化は、心筋細胞障害を引き起こすと考えられます。どうやらタンパク質分解システムは、抑制あるいは過剰に活性化されても細胞障害を引き起こすようです。今後は、このマウスを用いて様々な心疾患におけるオートファジー系の関わりを解明していきたいと考えています。
INFORMATION
お知らせ